Doc:Radiation/Phytoremediation
| もくじ | 基礎知識 | 自然放射線 | 人体への影響 | 胎児と子供 | ファイトレメディエーション | 土壌汚染 | 移行係数 | 食品汚染 | 家畜汚染 | Q&A とリンク |
文責: 有田正規 (東大・理・生物化学) 質問、コメント、誤り指摘、リクエスト等は arita@bi.s.u-tokyo.ac.jpまで
|
ファイトレメディエーションとは
植物を利用して土壌中の汚染物質を除去する手法をファイト(植物による)レメディエーション(修復)と呼びます。主に土壌中の重金属や農薬、石油等を対象にしますが、放射性物質を対象にしたファイトレメディエーションもあります[1]。大きく分けて二つの手法があります[2]。
- ファイトエクストラクション ... 成長が早く重金属等を蓄積しやすい植物を植えて、土壌から汚染物質を除く
- リゾフィルトレーション ... 同様の植物を用いて、水中の金属イオン等を水耕栽培により除く
- まとめ
- ファイトレメディエーションは、植物を数年だけ植えて汚染を除去するような技術というよりも、10~20年かけて汚染地の景観美化も含めながら対策を考える技術である
- 土壌中のセシウムはほとんどが表層 5cm にとどまる[3]
- 土壌中のセシウムを、植物を使って除染することは難しい [4]
- セシウムは土壌中のミネラル分と強固に結合してしまうので植物が簡単に利用できない
- 土壌中のミネラルと結合したセシウムを水溶させるには、土壌の酸性化やアンモニウムイオンの添加が有効
- セシウムはカリウム不足のときに植物が誤って取り込むため、肥沃な土地ほど除染は困難
- 植物によって蓄積できる金属の量や種類は大きく異なる (陸上植物葉の元素濃度一覧)
- 除染の効率を総合するとヒユ科の植物が優れている
- ヒマワリ(キク科)は、低濃度の汚染水から放射性物質を吸収するのには優れる
- イネ科は地上部を継続的に刈り取れるため、植物を植え続ける必要が無いところが利点
- 放射性核種を吸収した植物体は燃やして灰にする。高濃度のセシウムを含む灰の処分法を十分に考えてから実施すること
ファイトエクストラクション
重金属を多く蓄積する植物の一覧が、英語ウィキペディア上(植物名一覧, 金属と文献)にまとめられています。 植物の吸収する金属量は、土壌や栽培条件によって大きく異なります。実験用に用意された近交系でさえ水耕栽培と土植えでは蓄積される金属量は数倍以上異なります。また植物の器官によってもその量は異なり、相関を示しません[5]
鉛 Pb の場合
一般に鉛は植物が吸収できる形で土壌中に存在せず、pH 5.5-7.5 では Pb2+ は 10-8.5 M または 0.6 μg l-1 程度しか植物は利用できません。金属が溶出しやすいように土壌をEDTA (ethylene-dinitrilo-tetra-acetic acid)等で酸性にする必要があります。例えばカラシナ(Indian mustard)の場合、EDTA等を土壌に加えないで5週間ほど草丈を大きくし、その後EDTAを添加して土壌を酸性にしてから1週間ほど吸収させることで、植物体の乾燥重量にして1%程度の鉛を蓄積できます。
- 用いられる植物
| 植物学名 | 一般名 | 蓄積量 | 説明 |
|---|---|---|---|
| Thlaspi rotundifolium (L.) Graud.-Beaup | グンバイナズナの仲間 | 新芽に 8200 μg/g の鉛を蓄積[6] | イタリア北部の鉱山に自生する多年草。観賞用にもなる。草丈が 10cm と小さいために実用化は難しい |
| Brassica juncea (L.) Czern. | Indian mustard カラシナ | コントロールされた温室条件下では地上部の2% | 旺盛に成長するため応用が進んでいる |
セシウム Cs の場合
Dushenkov et al. 1999
Dushenkov S, Mikheev A, Prokhnevsky A, Ruchko M, Sorochinsky B 1999 "Phytoremediation of Radiocesium-Contaminated Soil in the Vicinity of Chernobyl, Ukraine" Environ Sci Technol 33, 469-475)
Plants were grown at the Northwest border of Chernobyl, Ukraine, approximately 10 km south of the ChNPP reactor. Bioaccumulation coefficient was calculated as a ratio of 137Cs in the plant versus 137Cs in the soil. The soil is a sod podzolic with a loamy-sand texture. Cesium is accumulated in the top 5cm layer and the trial was mede in 1996, 10 years after the Chernobyl accident.
| 植物学名 | 一般名 | 植物体Cs/土壌Cs | 除去できた総量 (Bq m-2) |
|---|---|---|---|
| Amaranthus retroflexus L. cv. PT-95 | アオゲイトウ | 1.50 | 3225 |
| Amaranthus retroflexus L. cv. aureus | アオゲイトウ | 1.90 | 2440 |
| Amaranthus retroflexus L. cv. belozernii | アオゲイトウ | 1.41 | 1392 |
| Amaranthus cruentus L. | スギモリケイトウ | 1.32 | 1251 |
| Helianthus tuberosus L. x Helianthus annuus L. | キクイモ、ヒマワリのかけあわせ | 0.49 | 1221 |
| Amaranthus caudatus L. | ヒモゲイトウ | 2.03 | 1144 |
| Amaranthus cruentus L. cv. myronivka | ヒモゲイトウ | 1.07 | 1053 |
| Helianthus tuberosus L. | キクイモ | 0.30 | 846 |
| Amaranthus hybridus L. | ホソアオゲイトウ | 0.60 | 719 |
| Amaranthus retroflexus L. cv. Antey | アオゲイトウ | 1.07 | 641 |
| Amaranthus tricolor L. 論文には A. bicolorと記載されているがおそらくtricolorの誤り。bicolorと記載しているのはこの論文の他にシーボルトコレクション。 |
ハゲイトウ | 0.59 | 417 |
| Amaranthus cruentus L. cv. paniculatus | ヒモゲイトウ | 0.53 | 412 |
| Zea mays L. | トウモロコシ | 0.28 | 409 |
| Helianthus annuus L. | ヒマワリ | 0.24 | 319 |
| Pisum sativum L. | エンドウマメ | 0.48 | 244 |
| Brassica juncea (L.) Czern. | カラシナ | 0.47 | 194 |
この報告では、セシウムの蓄積量がヒマワリ (H. annuus) よりもカラシナ (Brassica juncea) のほうが良く、除去できるセシウムの量はアマランサス(ヒユまたはケイトウ)類がヒマワリの10倍優れています。土壌にK+, EDTA, DTPA, Biogumusのような改良剤を入れても吸収量に変化はありません(ただしヒマワリだけはK+を増やすとCs吸収量がゼロに低下、カラシナは逆に向上)。根部には地上部の3∼4倍の放射性物質が蓄積、とあります。植物体の蓄積量は乾燥重量で1000 ∼ 3000 ベクレル/kg程度です。
Fuhrmann et al. 2002
Fuhrmann M, Lasat MM, Ebbs SD, Kochian LV, Cornish J (2002) "Uptake of Cesium-137 and Strontium-90 from Contaminated Soil by Three Plant Species Application to Phytoremediation" Plant and Environment Interactions 31, 904-909 植物はブルックハーベン国立研究所にある廃棄物処理の実験場で栽培。表層20cmのセシウム-137濃度は11.8 kBq/kg、ストロンチウム-90は0.06 kBq/kg。砂性の水はけのよい土壌。
| 植物学名 | 一般名 | 植物体Cs/土壌Cs | 植物体Sr/土壌Sr | Csを除去できた割合 |
|---|---|---|---|---|
| Brassica juncea (L.) Czern. | カラシナ | 0.46 | 8.2 | 0.078% |
| Amaranthus retroflexus L. | アオゲイトウ | 2.58 | 6.5 | 2.1% |
| Phaseolus acutifolius A. Gray | Tepary bean | 0.17 | 15.2 | 0.040% |
この報告では、植物体の収量が多いアオゲイトウ (redroot pigweed) が最もセシウム除去に適する結果となっており、上記のチェルノブイリにおける栽培結果とも一致しています。また、室内のコントロール下では硝酸アンモニウムを足すことでセシウムの吸収量が上がったのにもかかわらず[7]、屋外の実験では必ずしもそうならなかったと記されています。これはアンモニウムイオンの土壌における滞留時間が短いためと推測されています。カラシナでは土壌中のセシウム濃度がある値を超えると、その量と吸収量が比例しない現象が観察されています。
実験場付近に生育する植物の放射性物質吸収量は、マリーゴールド(Tagetes spp.) 17.7 kBq/kg, ササフラス (Sassafras albidum (Nutt.) Nees) 0.56 kBq/kg, セイタカアワダチソウ (Solidago spp.) 4.7 kBq/kg, その他の草に 2.6 kBq/kg でした。
モデルの妥当性には疑問を呈しながらも得られた結果をもとにファイトレメディエーションを実行した場合、ストロンチウムの(半減期は考慮しないで)半分を回収するのに7年、セシウムの半分を回収するのに18年かかると見積っています。
Entry et al. 2001
Entry JA, Watrud LS, Reeves M (2001) "Influence of organic amendments on the accumulation of 137Cs and 90Sr from contaminated soil by three grass species" Water, Air and Soil Pollution 126,385-398
植物はコントロールされた室内条件下で栽培。10x20 cm の排水口が無いプラスチック製容器の中で3ヵ月育てたあとに 3967 Bq Cs-137 または 4373 Bq Sr-90 を 10ml の水に混ぜて散布。土壌の放射線濃度はおおよそ 100+/-8 Bq/g Cs-137, 112+/-7 Bq/g Sr-90 とし、更に3ヵ月栽培して、草丈2.5cmより上を刈り取り。この収穫作業を2ヵ月おきに3回行い、地上部に蓄積されたCs量を計測。最後は根も取り出してCs量を計測。
| 肥料 | 植物学名 | 一般名 | 地上部に蓄積されたCs (3回の収穫合計)% |
根に蓄積されたCs(%) | Csを除去できた割合(%) |
|---|---|---|---|---|---|
| なし | Paspalum notatum | Bahia grass アメリカスズメノヒエ |
17.2 | 7.3 | 24.5 |
| なし | Sorghum halepense | Johnson grass セイバンモロコシ |
27.1 | 12.6 | 39.2 |
| なし | Panicum virgatum | Switchgrass スイッチグラス |
23.5 | 14.3 | 37.8 |
| ピート | Bahia grass | 29.1 | 14.5 | 43.6 | |
| ピート | Johnson grass | 40.8 | 22.0 | 62.8 | |
| ピート | Switchgrass | 32.9 | 14.9 | 47.8 | |
| 鶏糞 | Bahia grass | 25.3 | 11.2 | 36.5 | |
| 鶏糞 | Johnson grass | 67.3 | 32.4 | 99.7 | |
| 鶏糞 | Switchgrass | 39.4 | 14.9 | 54.3 |
ピートや鶏糞を施した場合は、植物の乾燥重量(バイオマス)が増え、結果としてセシウムやストロンチウムの吸収総量が増えています。栄養状態が良いと根を密に張り、養分の吸収が良くなるためと考えられます。また多くのセシウム(およびストロンチウム)が地上部に移動するため、刈り取ることで回収できています。数値をみるとセシウムおよびストロンチウムの回収率が極めて高いですが、Entryらは論文の末尾で屋外ではこの数値が達成できないことも記しています。
Entry らは、1996年にも論文をだしていますが[8]、こちらは総説に近く実データは記載されていません。後述しますが、正確さの観点からEntry の論文を私はあまり信用していません。
また、これより前にSaltらは室内でピート・ポドゾル土を用いた同様の実験をおこなっています[9]。Agrostis capillaris (西洋芝の一種) が、上部を定期的に刈り取ることでセシウムの多くを吸収すること、特に草の成長期に多く吸収することを示しています (冬季の蓄積量は夏季の3割減)。Saltらはスコットランドにおいてセシウムを蓄積する植物種も報告しています。
共通して報告されているのは、牧草の地上部を家畜が食べることでセシウムを多く摂取してしまう危険性です。食べる頻度が多いほど草も旺盛に成長してセシウムを多く吸収します。
Broadley & Willey 1997
Broadley MR, Willey NJ (1997) "Differences in root uptake of radiocaesium by 30 plant taxa" Environmental Pollution 97(1) 11-15
温室内で30種の植物を養分を与えずに1か月育て、その後放射性セシウム (CsCl) を 0.1 μ g/ g土壌 添加して 6 時間後にセシウムの吸収量を測っています。この論文は多くの文献に引用されていますが、セシウム添加後わずか 6 時間で測定しているという事実はあまり言及されていません。また論文中にはセシウムの吸収量は記載されておらず、図表から大まかに読み取れるだけです。
結論としてヒユ科 (Amaranthaceae) がイネ科よりも重さあたりセシウム吸収量が多いとしています。苗におけるセシウム量は苗の大きさにも相関しており、とりわけキノアやビートのセシウム吸収量が突出しています。
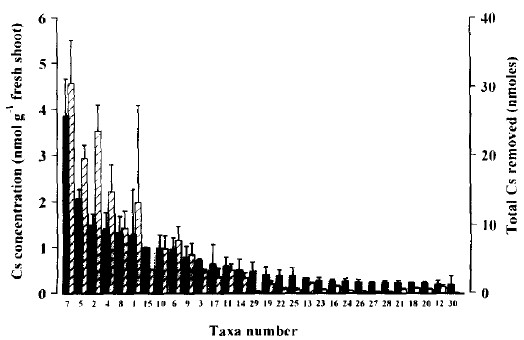
|
10 cm ポット苗におけるセシウム量. 10 μ mol CsCl を 20 ml 添加6時間後. エラー幅は標準偏差. |
| 番号 | 学名 | 和名 | 科名 | 苗の大きさ |
|---|---|---|---|---|
| 1 | Fagopyrum esculentum 論文にはPolygonum fagopyrumという旧名で記載 |
ソバ | Polygonaceae | 20.36 |
| 2 | Beta vulgaris ssp. maritima (L.) Arcang. | フダンソウ(ビート) | Amaranthaceae | 15.73 |
| 3 | Brassica nigra (L.) Koch | クロガラシ | Brassicaceae | 11.67 |
| 4 | Beta vulgaris ssp. vulgaris 'perpetural spinach' L. | フダンソウ(ビート) | Amaranthaceae | 10.59 |
| 5 | Beta vulgaris ssp. vulgaris 'italian chard' L. | フダンソウ(ビート) | Amaranthaceae | 5-10 |
| 6 | Beta vulgaris ssp. vulgaris 'cylindra' L. | フダンソウ(ビート) | Amaranthaceae | 5-10 |
| 7 | Chenopodium quinoa L. | キノア | Amaranthaceae | 5-10 |
| 8 | Beta vulgaris ssp. vulgaris 'detroit globe' L. | フダンソウ(ビート) | Amaranthaceae | 5-10 |
| 9 | Glycine max (L.) Mer. | ダイズ | Fabaceae | 5-10 |
| 10 | Lolium perenne L. | ホソムギ | Poaceae | 5-10 |
| 11 | Brassica oleraceae L. | キャベツ | Brassicaceae | 5-10 |
| 12 | Bromus lanceolatus Roth. | オオチャヒキ | Poaceae | 1-5 |
| 13 | Festuca rubra L. | オオウシノケグサ | Poaceae | 1-5 |
| 14 | Anthoxanthum odoratum L. | ハルガヤ | Poaceae | 1-5 |
| 15 | Atriplex patula L. | ハマアカザ | Amaranthaceae | 1-5 |
| 16 | Agrostis stolonifera L. | ハイコヌカグサ | Poaceae | 1-5 |
| 17 | Poa annua L. | スズメノカタビラ | Poaceae | 1-5 |
| 18 | Bromus sterilis L. | アレチノチャヒキ | Poaceae | 1-5 |
| 19 | Festuca elatior L. | ヒロハウシノケグサ | Poaceae | 1-5 |
| 20 | Leontodon hispidus L. | タンポポモドキ (属名) | Asteraceae | 1-5 |
| 21 | Trifolium pratense L. | アカツメクサ | Fabaceae | 1-5 |
| 22 | Danthonia spicata (L.) ex Roemer & Schultes | ?? | Poaceae | 1-5 |
| 23 | Festuca ovina L. | ウシノケグサ | Poaceae | 1-5 |
| 24 | Festuca juncifolia St.-Amans = F. arenaria |
Poaceae | < 1 | |
| 25 | Atriplex hortensis L. | ヤマホウレンソウ | Amaranchaceae | < 1 |
| 26 | Holcus lanatus L. | シラケガヤ | Poaceae | < 1 |
| 27 | NBromus erectus Huds. | ?? | Poaceae | < 1 |
| 28 | Festuca trachyphylla (Hack.) Krajina | ?? | Poaceae | < 1 |
| 29 | Festuca gigantea (L.) Vill. | オウシュウトボシガラ | Poaceae | < 1 |
| 30 | Koeleria macrantha (Ledeb.) Schultes | ミノボロ?? | Poaceae | < 1 |
論文における植物学名はあまり正確でなく、勝手に L. (リンネの意味) を添えていたり正式名がわからないものも多いです。 また30種のうち5種がビート、半分以上がイネ科という点で偏った選別になっています。ただし、対塩性が強い植物が金属イオンを無差別に取り込む傾向はセシウムについてもあてはまりそうです。
Coughtry et al. 1989
Coughtrey PJ, Kirton JA, Mitchell NG, Morris C (1989) "Transfer of radioactive caesium from soil to vegetation and comparison with potassium in upland grasslands" Environmental Pollution 62(4):281-315 PMID 15092335
Coughtryらはイギリス北西部・カンブリア地方における10地点の計測結果から1986年冬の時点で、降下したチェルノブイリ由来セシウムの4-19%が植物の地上部に蓄積しているとしています。 この文献を後日Entryらが各所で引用する際に4-19%がFestuca/Agrostis属に蓄積されると記述していますが、誤っています。Entryらの論文は表に誤記も多いうえ、引用文献で一貫して著者名を間違えていたり、引用文献の内容における数値を間違えていたりします。安易な孫引用には気をつけたほうが良いでしょう。(私であればこういう研究者の論文は信用しません。)
Broadley et al. 1999
Broadley MR, Willey NJ, Mead A (1999) "A method to assess taxonomic variation in shoot caesium concentration among flowering plants" Environ Pollut. 106(3):341-9 PMID 15093030
Broadley らが集めた、14のセシウム吸収研究のメタアナリシス(他の人が行った実験結果を総合的に判断したサマリー)です。植物の芽におけるセシウム量を比較し
という傾向が報告されています。蓄積量が圧倒的に多いのは、アマランサス・キヌアという雑穀、次いでビート・菜の花類(特にコールラビ、サヴォイキャベツなど)・キュウリとなっています。ナス科、イネ科、セリ科、キク科などは低くなっています。個人的には、移行係数が栽培条件で大きく異なるので順番や数値にあまり説得力はないと感じます。
リゾフィルトレーション
植物の水耕栽培により水中の汚染物質を除去する手法を、リゾフィルトレーションと呼びます。根の表面積が大きいほうが有利なので、ヒマワリやイネ科の植物など根を密に張る植物が用いられます。
セシウム Cs の場合
- 実験されている植物
| 植物名 | 蓄積量 | 説明 |
|---|---|---|
| Helianthus annus L. ヒマワリ (キク科) |
|
多くの実験はおおよそヒマワリ 1本あたり1リットル以下という大変密度の高い状況でおこなわれています。実際に汚染水を貯蔵した池などで実験をする際には、ポンプ等で汚染水をまんべんなく循環させ、ヒマワリの根に触れさせる必要が生じます。この条件さえ満たせれば、逆に、効率よくセシウムを吸収できるとも考えられます。
セシウムが蓄積される部位ですが、文献[10]では根の部分、文献[11]では若芽など成長が速い部分となっています。これはヒマワリの成長度合いによる差と考えられます。後者の文献では小さなヒマワリを高濃度のセシウム下で育てているため、回収率が前者より低くなっています。 |
| Calotropis gigantea R.Br. (キョウチクトウ科) | 10 ml の汚染水から、5 × 103 kBq/l の 90Sr および 137Cs を168時間後にそれぞれ 97%, 44% 吸収[12] | 南インド・ケララ地方のモナド石が出る地域に自生する多年性植物で、トリウムをよく吸収する(ウィキペディアのリンク)。Milkweedの名の通り、白い乳液(ラテックス)を出す。放射性物質は根の部分に多く蓄積。実験条件は汚染水に対し植物体の量が極めて多く、樹木を用いている点でも実用化は困難と思われる。 |
| Vetiveria zizanoides L. Nash (now Chrysopogon zizanoides) | 10 ml の汚染水から、5 × 103 kBq/l の90Sr および 137Cs を168時間後にそれぞれ 94%, 61% 吸収[13] | Vetiveriaは土壌流出を防ぐために用いられる重要な植物。実験条件は汚染水に対し植物体の量が極めて多い。イネ科の植物は重金属の回収などにもよく用いられる。 |
セシウム回収の難しさ
集めた植物体の処分
このページで紹介される植物を用いてセシウムを回収した場合、(栽培条件にも大きく左右されますが)汚染土壌と同程度のベクレル数に達する植物の乾燥体が得られます。これを、通常ゴミとして廃棄したり、自分で焼却して灰を適当に撒いたりしてはいけません。放射性廃棄物専用の焼却炉を用意して、高濃度のセシウムを含む灰を保管する設備を整えてください。
とりわけ、灰の処分法を考えないで実施した場合は高濃度放射性廃棄物を一般ごみや田畑に混ぜ込む危険性があり、セシウム被害をむしろ広げる可能性がある点に十分注意してください。
土壌のミネラル分との関係
セシウム-137の回収を難しくするのは、その不溶性 (< 0.3% が水溶性) です。有機酸や界面活性剤を土壌に混ぜても溶出せず、5 M の硝酸を過剰に加え、ようやく 20.7% を回収できる程度です。
セシウムの多くは土壌中のミネラル類と強固に結合していると考えられます。詳しくは土壌とセシウムの項をごらんください[4]。粘土質の土壌では植物中のセシウム量が少なく、泥炭地や砂地では植物中のセシウム量が増えることが一貫して報告されています。また、土を耕してセシウムを拡散させると植物体での蓄積量は減ります。また粘土中のミネラル分にセシウムが吸着する度合いは時間と共に進み、とりわけ雲母 (mica) に吸着されたセシウムは植物も利用できません。
カリウムおよびアンモニアとの関係
セシウムはカリウムと競合するので、カリウムが多い土壌では植物体における蓄積量が下がることが一貫して報告されています。 アンモニウムイオンが、土壌のミネラル分に吸着されたセシウムイオンを追い出すことも報告されていますが、アンモニア肥料を施すことが植物中のセシウム量を増やすかどうかは報告によって結果がまちまちです[14]。
- 屋内のコントロール条件下で、硝酸アンモニウム、塩化アンモニウムを土壌改良材として用いると、キャベツ、カラシナなど複数の植物でセシウム量が増加すること報告されています。ただし量によっては植物の生長も妨げられます。
- 屋外では、アンモニウムイオンの効果が観測されません (Fuhrmann et al. の項を参照)
- 2日間の実験ではNH4+やK+を増やすと植物体へのセシウム移行量が減るという報告もあります[15]
- 参考文献
- ↑ Dushenkov S (2003) Trends in Phytoremediation of radionuclides Plant and Soil 249:167-175
- ↑ Dushenkov S, Kapulnik Y, Blaylock M, Sorochisky B, Raskin I, Ensley B (1997) "Phytoremediation: a novel approach to and old problem" In Global Environ Biotechnol (D.L. Wise Ed.) 563-572
- ↑ Rosen K, Oborn I, Lonsjo H "Migration of radiocaesium in Swedish soil profiles after the Chernobyl accident, 1987–1995" J Environ Radiology" 46(1), 45-66 journal link
- ↑ 4.0 4.1 日本土壌肥料学会によるセシウムの作物(特に水稲)系での動きに関する基礎的知見も参考にしてください。
- ↑ Ghandilyan A et al. (2009) "A strong effect of growth medium and organ type on the identification of QTLs for phytate and mineral concentrations in three Arabidopsis thaliana RIL populations" J Exp Bot. 60(5):1409-25
- ↑ Reeves RD, Brooks RR 1983 "Hyperaccumulation of lead and zinc by two metallophytes from mining areas in Central Europe" Environ Pollut Ser A 31:277-285
- ↑ Lasat MM, Norell WE, Kochian LV (1997) Potential for phytoextraction of 137Cs from a contaminated soil" Plant Soil 195:99-106
- ↑ Entry JA, Vance NC, Hamilton MA, Zabowski D, Watrud LS, Adriano DC (1996) "Phytoremediation of soil contaminated with low concentrations of radionuclides" 'Water Air and Soil Pollution 88, 167-176
- ↑ Salt CA, Kay JW, Donaldson L, Woolsey JM (1997) "The influence of defoliation intensity, season and leaf age on radiocaesium concentrations in Agrostis capillaris" Journal of Applied Ecology 34:1177-1189
- ↑ 10.0 10.1 Dushenkov S, Vasudev D, Kapulnik Y, Gleba D, Fleisher D, Ting KC, Ensley B 1997 "Removal of Uranium from Water Using Terrestrial Plants" Environ Sci Technol 31:3468-74
- ↑ 11.0 11.1 Soudek P, Valenova S, Vavrikova Z, Vanek T (2006) "137Cs and 90Sr uptake by sunflower cultivated under hydroponic conditions" J environ Radioactivity 88:236-250
- ↑ Eapen S, Singh S, Thorat V, Kaushik CP, Raj K, D'Souza SF (2006) "Phytoremediation of radiostrontium 90Sr and radiocesium 137Cs using giant milky weed (Calotropis gigantea R.Br.) plants" Chemosphere 65:2071-2073
- ↑ Singh S, Eapen S, Thorat V, Kaushik CP, Raj K, D'Souza SF (2008) "Phytoremediation of 137cesium and 90strontium from solutions and low-level nuclear waste by Vetiveria zizanoides" Ecotoxicology and Environmental Safety 69:306-311
- ↑ Zhu YG, Smolders E (2000) "Plant uptake of radiocaesium: a review of mechanisms, regulation and application" Journal of Experimental Botany 51(351): 1635-1645
- ↑ Shaw G, Hewamanna R, Lillywhite J, Bell JNB (1992) Radiocaesium uptake and translocation in wheat with reference to the transfer factor concept and ion competition effects J Environ Radioactivity 16, 167-180