Aritalab:Lecture/Biochem/Isotope
From Metabolomics.JP
同位体
同じ原子でも(同じ原子とは原子番号が同じ、つまり陽子の数が同じこと)、質量数が異なる核種を同位体 (isotope)といいます。質量数は元素記号の左肩に書く慣わしで、炭素13は 13C と書きます。 同位体には、放射線を出して崩壊する放射性同位体 (radioisotope) と、時間を経ても割合が変化しない安定同位体 (stable isotope) があります。炭素13は安定同位体ですが、炭素14は放射性同位体です(半減期約5730年)。 安定同位体は自然界において一定の割合を示しますが、地球環境や食物連鎖によっと微妙な差が出てきます。その差を安定同位体比と呼び、質量分析計で計測できます。
- 例
- 炭素13の安定同位体比 δ13C =
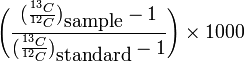 ‰
‰
記号は通常パーミル ‰ (permille) を用い、1 ‰ とは 1/1000 を意味します。 天然物の主要な元素である炭素 C, 水素 H, 酸素 O, 窒素 N に重要な安定同位体は以下のとおりです。
- 炭素
- 生物が炭素を固定する経路の差を反映して、-40 ‰ ~+4 ‰ という比較的大きな変化を示します。
- 水素と酸素
- 水が蒸発する際に軽い安定同位体のほうが気化しやすく、気候や地域によって大きく変動します。変動は大きくので、安定同位体比から地域を特定することは難しいでしょう。
- 窒素
- 有機肥料など生物由来の窒素源で育てた野菜は平均 +8 ‰、化学肥料で育てた野菜は平均 + 3 ‰程度の変化を示します。[1]ただし、ばらつきも大きく安定同位体比から有機栽培かどうかを判定することは困難です。
以上の理由から、バイオマーカーとして利用されるのは主に炭素です。
- 参考文献
- ↑ 法邑ら 「窒素安定同位体比を用いた化学肥料使用判別法の検討」(独)農林水産消費安全技術センター http://www.famic.go.jp/technical_information/investigation_research_report/pdf/3202.pdf